Potencjalne błędy popełniane w trakcie badania nasienia przy ocenie żywotności plemników
30 stycznia 2019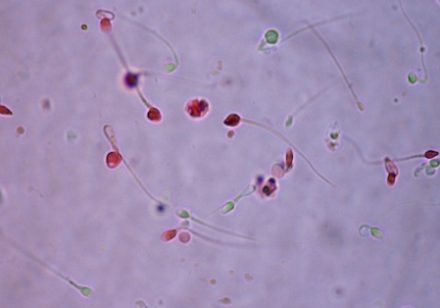
Ze względu na to, że badanie nasienia, zarówno wykonywane metodą manualną jak i komputerowo wspomaganą jest oceną wieloczynnikową, kilkuetapową, subiektywną, jego wykonanie jest niestety „narażone” na błędy. A ponieważ znane wszystkim przysłowie głosi, że człowiek uczy się na błędach, dobrze byłoby o tych potencjalnych błędach przynajmniej pomyśleć. Dlatego poniżej przedstawiamy listę błędów, których popełnienie przy ocenie koncentracji, liczby plemników, ich morfologii, żywotności czy ruchliwości może zafałszować uzyskiwane przez nas w pocie czoła wyniki – lista opracowana jest na podstawie zaleceń WHO oraz własnych doświadczeń. Niektóre z nich wynikają z bardzo błahych powodów, o których często zapominamy, nie zdajemy sobie z nich sprawy lub po prostu ignorujemy. Myślę, że po przeczytaniu tego opracowania niejeden doświadczony diagnosta złapie się za głowę ze słowami „(…) że ja tego wcześniej nie zauważyłam/em!” (co było zresztą i moim udziałem przy opracowywaniu tej listy)… jednocześnie z góry gratuluję tym czytelnikom, którzy żadnego z tych błędów nie popełniają.
Poniżej lista potencjalnych błędów popełnianych w trakcie badania nasienia przy ocenie żywotności plemników:
– niedostateczne wymieszanie próbki przed wykonaniem preparatu;
– niewłaściwe wykonanie preparatu – za gruby lub zbyt cienki preparat (szczególnie w przypadku preparatu zbyt grubego napotykamy na problemy tj. zbyt wiele plemników na raz co utrudnia ocenę, powoduje ich nakładanie się, niekontrolowane przemieszczanie się poza pole i do pola widzenia; niemożliwość analizowania wszystkich płaszczyzn fokalnych preparatu jednocześnie, co spowoduje wydłużenie czasu analizy (konieczność nadmiernego kręcenia śrubą mikrometryczną), a także możliwość pominięcia niektórych plemników; poza tym plemniki nieruchliwe będą opadać na dno preparatu i w zależności od tego czy będziemy oglądać tę płaszczyznę czy też nie zostaną pominięte w ocenie);
– zbyt długie oczekiwanie z oceną preparatu po jego wykonaniu lub zbyt długi czas wykonywania analizy (żywotność może się obniżać z upływem czasu i obsychaniem preparatu);
– wykonywanie analizy zbyt późno od czasu oddania nasienia i jego upłynnienia (co może powodować wzrost odsetka plemników martwych);
– zliczanie plemników „napływających” do pola widzenia – powoduje przeszacowanie liczby plemników żywych (jako że plemniki wykazujące zdolność ruchu na pewno są żywe);
– nieprawidłowa temperatura stolika lub otoczenia (szczególnie zbyt wysoka temperatura może uszkodzić plemniki i spowodować ich nadmierne obumarcie);
– analizowanie zbyt blisko krawędzi szkiełka (plemniki częściej tam obumierają z powodu obsychania preparatu);
– kończenie zliczania na wielokrotności 100 podczas gdy całe wybrane pole widzenia nie jest jeszcze ocenione;
– brak zastosowanie metod umożliwiających zmniejszenie ocenianego pola (np. siatki czy podział pola widzenia na ćwiartki na obiektywie mikroskopu) co ma szczególne znaczenie przy dużej koncentracji i ruchliwości plemników;
– nielosowy wybór pola do oceny (np. wyszukiwanie pól „łatwiejszych do zliczenia” lub takich gdzie są/nie ma plemników ruchliwych;
– ocena w zbyt małej liczbie pól widzenia (np. przy preparacie o dużej koncentracji plemników ocena tylko w jednym polu);
– błędy matematyczne (np. przy wyliczaniu odsetka pojawiające się w przypadkach kiedy zliczanie jest do liczby innej niż wielokrotności 100);
– niesprawny sumator (np. zacinający się sumator może doprowadzić do tego, że część plemników nie zostanie uwzględniona w obliczeniach, pomimo iż osobie oceniającej wydaje się, że je policzyła; niesprawny jeden przycisk sumatora może spowodować zafałszowanie uzyskanego odsetka);
– używanie niewłaściwego powiększenia i oświetlenia w mikroskopie (powoduje, że trudno odróżnić kolory);
– niewłaściwa metoda barwienia (w niektórych przypadkach warunki hypo-osmotyczne powodują zabijanie plemników);
– ponowne nawodnienie wysuszonego preparatu (przy metodach z preparatami utrwalonymi np. eozyna – nigrozyna) powodujące wnikanie barwnika do plemników, a przez to nieprawidłową ich kwalifikację;
– ocenianie plemników z blado różowymi główkami jako martwe (i przeszacowywanie odsetka martwych plemników);
– ocena plemników z czerwonym/różowym zabarwieniem wstawki lub szyjki jako martwe (i przeszacowywanie odsetka martwych plemników);
– uzyskanie niższego wyniku żywotności plemników, niż wynik całkowitej ruchliwości plemników (żywotność plemników zawsze musi być większa lub równa od ruchliwości całkowitej plemników, ponieważ plemniki ruchliwe nie mogą być jednocześnie martwe… w przypadku uzyskania takiego wyniku jedna z analiz została wykonana nieprawidłowo);
– wyciąganie średniej do podania ostatecznego wyniku z dwóch zliczeń nadmiernie się od siebie różniących.
Zobacz także listy potencjalnych błędów popełnianych przy ocenie innych parametrów w trakcie badania nasienia:
Potencjalne błędy popełniane przy ocenie koncentracji plemników i całkowitej liczby plemników
Potencjalne błędy popełniane w trakcie badania nasienia przy ocenie morfologii (budowy) plemników
Potencjalne błędy popełniane w trakcie badania nasienia przy ocenie ruchliwości plemników
Opracowanie: Eliza Filipiak (dr n. med.)
Z0BACZ TAKŻE

Błędy najczęściej popełniane przy interpretacji wyniku ogólnego badania nasienia
Sama analiza nasienia nie jest zadaniem prostym, tak samo jak nie zawsze prosta jest interpretacja... Więcej →

Potencjalne błędy popełniane w trakcie badania nasienia przy ocenie koncentracji plemników i całkowitej liczby plemników
Jak wiadomo, manualna (ale także komputerowo wspomagana) analiza nasienia (badanie nasienia) jest oceną... Więcej →

Standaryzacja badania nasienia – czy polskie laboratoria mają z tym problem?
Badanie nasienia jest jednym z badań, które ze względu na swoją złożoność nastręczają problemów... Więcej →

Program Międzylaboratoryjnej Kontroli Jakości Badania Ogólnego Nasienia SpermControl
O Programie Międzylaboratoryjnej Kontroli Jakości Badania Ogólnego Nasienia SpermControlCo obejmuje Program... Więcej →

Interpretacja wyników badania nasienia
Wynik badania ogólnego nasienia oceniać powinno się wykorzystując wytyczne np. WHO (Światowej Organizacji... Więcej →
Potencjalne błędy popełniane w trakcie badania nasienia przy ocenie morfologii (budowy) plemników
Może być tak, że po przeczytaniu tego opracowania niejeden doświadczony diagnosta złapie się za głowę ze... Więcej →
